L’azote est un paradoxe planétaire. Il domine l’atmosphère terrestre — environ 4 × 10⁶ Gt sous forme de N₂, soit près de 75 % de sa masse et 78 % de son volume. Il a toujours été très abondant mais, chimiquement inerte, il est resté longtemps indisponible pour la vie.
Aujourd’hui, le problème s’est inversé : ce n’est plus le manque d’azote qui contraint la biosphère, mais l’excès d’azote réactif1 que les activités humaines injectent dans les sols, les eaux et l’atmosphère.
1. Aux origines : un azote abondant mais chimiquement verrouillé
À l’échelle cosmique et planétaire, l’azote est un élément banal. Il est incorporé dans les matériaux primitifs qui forment la Terre, puis dégazé vers l’atmosphère lors des premières phases volcaniques. Dès les premiers milliards d’années, le diazote (N₂) devient ainsi un constituant dominant de l’atmosphère terrestre.
Mais cette abondance est trompeuse. Le N₂ est une molécule extrêmement stable, liée par une triple liaison (N≡N) qui requiert une énergie considérable pour être rompue. Cette inertie chimique explique pourquoi, malgré sa profusion, l’azote est longtemps resté indisponible pour la biosphère naissante.
Dans les environnements prébiotiques, les premières formes d’azote réactif (NOx, NH₃) sont produites par des processus abiotiques : éclairs, rayonnement ultraviolet, chimie hydrothermale. Ces flux d’azote réactif sont extrêmement faibles, de l’ordre de 0,005 Gt N/an pour la foudre, et du même ordre pour la photolyse et chimie atmosphérique. L’azote réactif représente une fraction infinitésimale du réservoir total.
Ce déséquilibre structure profondément les conditions d’émergence de la vie : l’azote est en fait une contrainte géochimique majeure. Certaines études2 suggèrent que ces faibles flux abiotiques ont néanmoins suffi à alimenter la chimie prébiotique, notamment via la formation de nitrates ou d’ammoniac dans les océans primitifs, produits par la foudre, le rayonnement ultraviolet ou la chimie hydrothermale.
Mais à ce stade, il n’existe pas encore de “cycle” au sens strict : l’azote suit des trajectoires ouvertes, lentes, dominées par la physique et la géochimie. Les reconstructions isotopiques3 suggèrent que l’azote circule depuis les premiers âges de la Terre entre manteau, croûte et atmosphère. Il s’agit donc plutôt d’un système ouvert, lent, dominé par la géochimie.
2. L’invention biologique : la révolution microbienne de l’azote
2.1 La fixation bactérienne de l’azote atmosphérique
Le véritable basculement intervient avec l’évolution des micro-organismes capables de fixer l’azote atmosphérique. Cette innovation, probablement très ancienne (plus de 3 milliards d’années), repose sur une enzyme unique : la nitrogénase. Cette enzyme permet de convertir le N₂ en ammoniac (NH₃), une forme directement intégrable dans les acides aminés et les nucléotides. C’est un processus énergétiquement coûteux, mais décisif car il ouvre l’accès à un réservoir d’azote quasi illimité comme on l’a vu.
Avec cette innovation, le cycle de l’azote devient véritablement biogéochimique, c’est-à-dire qu’il est contrôlé par des micro-organismes et implique des transformations chimiques multiples. En effet, l’azote peut exister sous de nombreuses formes chimiques4, de l’ammoniac aux nitrates. Les micro-organismes utilisent les transformations entre ces formes comme sources d’énergie, ce qui permet de “faire circuler” l’azote dans la biosphère.
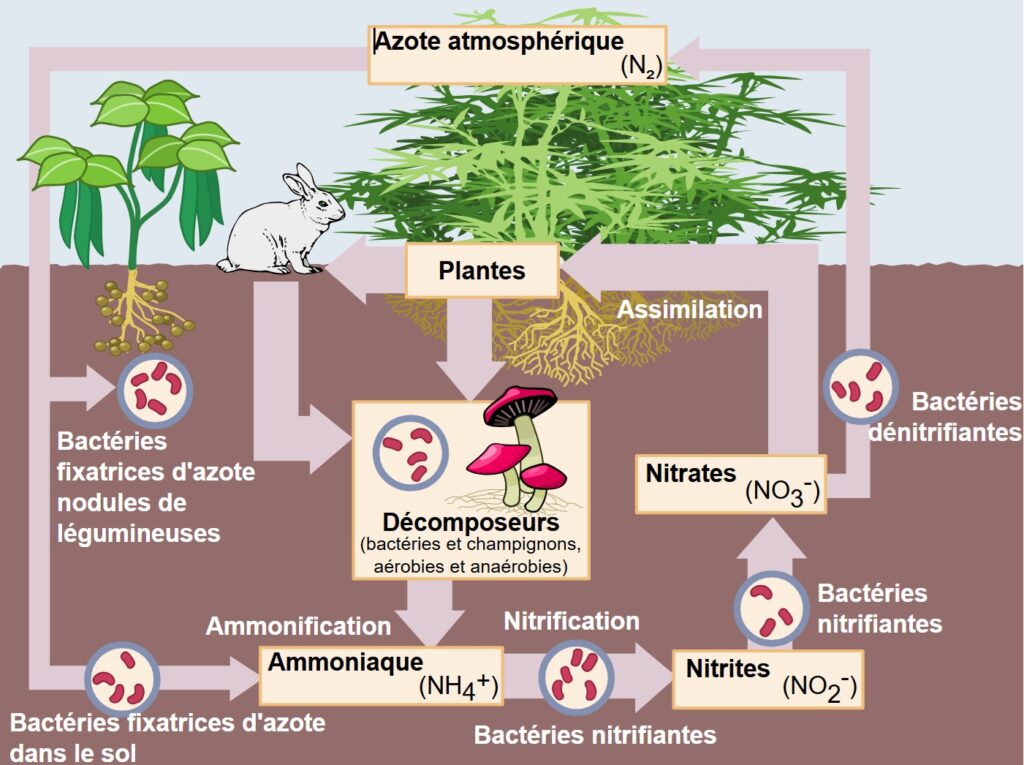
Ce cycle repose sur une série de processus microbiens interconnectés :
- Fixation de l’azote : N₂ → NH₃ (ammoniac).
Certaines bactéries et cyanobactéries captent l’azote atmosphérique et le transforment en ammoniac, une forme assimilable par les plantes. Par exemple, les rhizobiums dans les nodules de légumineuses réalisent cette fixation.
- Nitrification (NH₃ → NO₃⁻).
L’ammoniac est oxydé en nitrites puis en nitrates par des bactéries nitrifiantes (Nitrosomonas, Nitrobacter). Ce processus nécessite la présence d’oxygène. C’est un exemple typique de cycle oxydatif de l’azote.
- Assimilation biologique.
Les plantes absorbent l’ammonium (NH₄⁺) ou les nitrates (NO₃⁻) et les incorporent dans leurs protéines et acides nucléiques, permettant le transfert d’azote dans la biosphère.
- Ammonification (matière organique → NH₄⁺).
Les bactéries et champignons décomposent la matière organique (déchets, cadavres) et libèrent de l’ammonium, bouclant le cycle de l’azote.
- Dénitrification (NO₃⁻ → N₂).
Dans les milieux anoxiques, certaines bactéries réduisent les nitrates en azote gazeux. Le produit final est principalement N₂, mais une partie peut être libérée sous forme de N₂O, un puissant gaz à effet de serre. Ce processus complète le cycle anaérobie de l’azote et joue un rôle important dans le retour d’azote vers l’atmosphère.
Dans les milieux anoxiques, certaines bactéries réduisent les nitrates en azote gazeux, qui retourne dans l’atmosphère. Ce processus complète le cycle anaérobie de l’azote.
Ainsi, l’azote circule entre l’atmosphère, le sol, les plantes et les micro-organismes, passant par différentes formes chimiques selon les cycles microbiens qui le régulent.
2.2 La révolution de l’oxygène
Un second tournant majeur survient avec la Grande Oxydation (~2,4 Ga) (voir le post Homo sapiens face à Gaïa 1/3 : dynamiques planétaires et crises du vivant §13). L’apparition durable d’oxygène atmosphérique transforme profondément le cycle de l’azote5 :
- Activation de la nitrification : la présence d’O₂ permet aux bactéries nitrifiantes d’oxyder l’ammoniac en nitrites puis en nitrates6, (cf ci-dessus) un processus qui était impossible dans une atmosphère anoxique. Cette étape crée de nouvelles formes d’azote disponibles pour les plantes et le phytoplancton.
- Intensification de la dénitrification : parallèlement, dans les zones anoxiques comme les sédiments profonds ou les eaux stagnantes, certaines bactéries utilisent les nitrates comme accepteurs d’électrons, produisant du N₂ ou du N₂O qui retourne dans l’atmosphère. La dénitrification devient ainsi un élément majeur du cycle global de l’azote.
- Complexification des rétroactions : l’oxygène relie désormais le cycle de l’azote à ceux du carbone et du soufre. Par exemple, l’oxydation du NH₄⁺ en NO₃⁻ produit de l’énergie utilisée par des bactéries autotrophes, qui fixent du CO₂ en matière organique, montrant que les cycles sont intimement couplés.
Le cycle de l’azote devient ainsi un système dynamique, où les transformations dépendent des équilibres redox locaux7. Selon ces conditions chimiques, certaines réactions sont favorisées tandis que d’autres sont inhibées :
- En milieu oxydant (riche en O₂), la nitrification peut se produire : l’ammoniac (NH₃) est oxydé en nitrites (NO₂⁻) puis en nitrates (NO₃⁻) par des bactéries nitrifiantes.
- En milieu réducteur ou anoxique (pauvre en O₂), la dénitrification se produit : les nitrates sont réduits en N₂ ou N₂O par des bactéries dénitrifiantes8.
- L’assimilation biologique et l’ammonification se produisent dans des conditions variées, mais restent également modulées par la disponibilité d’oxygène et d’autres composés chimiques.
Ainsi, l’azote circule entre atmosphère, eau et sols de manière régulée, et le cycle reste adaptatif aux variations environnementales. En d’autres termes, la vie ne se contente pas d’utiliser l’azote : elle façonne activement les conditions chimiques et écologiques qui rendent possible sa propre fertilité, en orchestrant un réseau complexe de transformations microbiennes et chimiques.
3. Un cycle lent et autorégulé : l’azote comme contrainte structurante
Une fois ce réseau microbien établi, le cycle de l’azote atteint une forme d’équilibre dynamique qui va perdurer pendant des milliards d’années, tout en étant continuellement réajusté par les grandes transitions de l’histoire de la Terre9 (oxygénation, évolution biologique, perturbations climatiques).
Dans ce régime préindustriel, un point est fondamental : la production d’azote réactif est limitée par la fixation biologique, elle-même contrainte par l’énergie disponible et les conditions écologiques. Cela fait de l’azote le nutriment limitant principal dans de nombreux écosystèmes terrestres et marins10.
Ce rôle limitant a des conséquences profondes. Il contrôle la productivité primaire (donc le cycle du carbone), structure les communautés microbiennes et végétales et impose des rétroactions stabilisatrices à l’échelle globale11.
Les études modernes montrent que ce cycle fonctionne comme un système régulé par des bilans entrée/sortie. L’entrée c’est principalement la fixation biologique et la sortie, la dénitrification (retour à N₂). Ces flux tendent à s’équilibrer sur le long terme, ce qui confère au cycle une résilience remarquable face aux perturbations naturelles. Dans les océans notamment12, des mécanismes de rétroaction stabilisent la disponibilité en azote : une augmentation de l’azote disponible peut stimuler la dénitrification, limitant ainsi les excès.
Mais cette stabilité a un prix : elle repose sur des vitesses de transformation relativement lentes, à l’échelle des temps géologiques ou écologiques. Pendant des millions d’années, l’azote a agi comme un régulateur invisible de la biosphère : il a freiné la vie autant qu’il l’a rendue possible.
4. Le couplage des cycles biogéochimiques
Le cycle de l’azote ne fonctionne pas de manière isolée, mais s’inscrit dans un réseau étroitement couplé de cycles biogéochimiques, en particulier ceux du carbone, du phosphore et de l’eau. Ces interactions reposent à la fois sur les métabolismes microbiens et sur les propriétés physiques des milieux.
Le lien avec le cycle du carbone ( voir le post Homo sapiens face à Gaïa 1/3 : dynamiques planétaires et crises du vivant, §1.1.1) est fondamental : de nombreuses transformations de l’azote sont directement couplées aux flux de carbone. Par exemple, la nitrification fournit de l’énergie à des micro-organismes autotrophes capables de fixer le CO₂, tandis que la dénitrification, qui se déroule dans des milieux anoxiques riches en matière organique, utilise le carbone comme source d’électrons. Inversement, la disponibilité en azote conditionne la production primaire, donc la capacité des écosystèmes à fixer et stocker le carbone.
Le phosphore joue quant à lui un rôle de facteur limitant. Indispensable à la synthèse de l’ADN, de l’ATP et des membranes cellulaires (voir le post L’Anthropocène : l’humanité une force « phosphorique »), il contrôle la croissance des organismes et donc l’intensité des transformations de l’azote et du carbone. À l’échelle des écosystèmes, la disponibilité relative en azote et en phosphore détermine souvent la productivité biologique et les équilibres trophiques.
Le couplage avec le cycle de l’eau est tout aussi essentiel. L’eau agit comme un vecteur de transport des formes azotées (notamment le lessivage des nitrates vers les rivières et les océans), mais elle contrôle aussi les conditions d’oxygénation des milieux. Des sols saturés en eau deviennent anoxiques, favorisant la dénitrification, tandis que des sols bien drainés et oxygénés favorisent la nitrification. Ainsi, les régimes hydriques déterminent en grande partie quelles transformations de l’azote peuvent se produire localement. Ces cycles sont enfin également liés à celui du soufre, notamment dans les milieux anoxiques, où les micro-organismes utilisent successivement différents accepteurs d’électrons. Lorsque les nitrates sont consommés par la dénitrification, les sulfates peuvent à leur tour être réduits, illustrant la continuité des processus redox qui couplent les cycles de l’azote, du carbone et du soufre. Ces différents cycles sont liés par des contraintes redox13 communes : la disponibilité en oxygène, elle-même dépendante de la circulation de l’eau et de l’activité biologique, régule simultanément les transformations de l’azote, du carbone et du soufre.
Ce couplage s’est renforcé au cours de l’histoire de la Terre, notamment avec la colonisation des continents par les plantes (voir Homo sapiens face à Gaïa 1/3 : dynamiques planétaires et crises du vivant §15), qui a profondément modifié le cycle de l’eau (évapotranspiration, formation des sols, rétention d’humidité) et, par conséquent, les conditions dans lesquelles se déroulent les transformations de l’azote et du carbone.
5. L’invention de l’azote industriel et le franchissement d’une limite planétaire
La relative stabilité du cycle de l’azote est profondément bouleversée au début du XXᵉ siècle avec une innovation technologique majeure : procédé Haber-Bosch. Développé par Fritz Haber pour démontrer la synthèse d’ammoniac à partir d’azote atmosphérique et d’hydrogène, puis industrialisé par Carl Bosch, ce procédé permet la production industrielle à grande échelle d’ammoniac synthétique. La synthèse d’ammoniac est devenue la principale source d’azote assimilable pour les engrais modernes. Selon l’expert Vaclav Smil14, cette invention est l’une des plus importantes du XXᵉ siècle, car elle a transformé radicalement l’agriculture, multiplié les rendements des cultures et rendu possible l’explosion démographique mondiale en fournissant de vastes quantités d’azote fertilisant les sols à une échelle auparavant inimaginable pour l’agriculture traditionnelle : sans cette source d’azote synthétique, les approvisionnements alimentaires de la population mondiale actuelle ne seraient pas réalisables.
Mais cette transformation marque un basculement fondamental : l’humanité devient une force géochimique. Aujourd’hui, les activités humaines ont plus que doublé15 les flux d’azote réactif dans la biosphère. Une part considérable de l’azote présent dans les organismes vivants (y compris dans nos propres corps) provient désormais de cette synthèse industrielle. L’azote réactif est désormais produit à grande échelle par les engrais agricoles, l’élevage intensif, la combustion des énergies fossiles et certains procédés industriels.
Ce surplus d’azote dépasse largement les capacités d’absorption des écosystèmes. Il s’accumule alors dans les sols, les eaux et l’atmosphère.Les conséquences sont multiples : pollution des eaux par les nitrates, eutrophisation (prolifération d’algues, zones mortes), émissions de protoxyde d’azote (N₂O), un puissant gaz à effet de serre, dégradation des sols et perte de biodiversité. L’azote, autrefois facteur limitant est devenu un facteur de déséquilibre. Les scientifiques considèrent aujourd’hui que le cycle de l’azote fait partie des limites planétaires déjà largement dépassées16. Ce dépassement est particulièrement critique car il agit en cascade. Il perturbe les écosystèmes aquatiques, modifie les cycles du carbone et du climat, affecte la qualité de l’air et la santé humaine et contribue à l’érosion de la biodiversité.
Contrairement au carbone, dont les effets sont globaux, l’azote agit souvent de manière diffuse, locale et cumulative — ce qui le rend moins visible, mais potentiellement tout aussi déstabilisant.
Conclusion : maîtriser l’azote, ou subir ses effets
L’histoire du cycle de l’azote est celle d’une contrainte devenue levier, puis d’un levier devenu perturbation. Le basculement d’origine humaine est considérable.
Comme pour le phosphore ou le carbone, la question n’est pas de supprimer l’usage de l’azote — indispensable à la vie et à l’agriculture — mais de le réinscrire dans des cycles compatibles avec les capacités de la biosphère. Cela suppose une transformation des systèmes agricoles, une réduction des excès d’engrais, une meilleure gestion des effluents, et plus largement, une redéfinition de notre rapport aux flux de matière.
Car dans l’Anthropocène, l’humanité n’est plus seulement une espèce : elle est devenue une force biogéochimique.
Alain Grandjean
Notes
- On appelle azote réactif (Nr) l’ensemble des composés azotés autres que le N₂, incluant les formes minérales, organiques et gazeuses, capables de circuler rapidement dans la biosphère et de participer aux processus biologiques et chimiques. Les principales formes d’azote réactif sont les formes réduites (ammoniac (NH₃), ammonium (NH₄⁺)), les formes oxydées (nitrates (NO₃⁻), nitrites (NO₂⁻), oxydes d’azote (NOₓ)), les formes gazeuses actives (protoxyde d’azote (N₂O) ) et l’ azote organique (acides aminés, protéines, matière vivante). Voir Galloway et al. (2008), Transformation of the nitrogen cycle : recent trends, questions potential solutions, Science. ↩︎
- Voir les articles suivants : Stüeken, E. E., Kipp, M. A., Koehler, M. C., & Buick, R. (2016). The evolution of Earth’s biogeochemical nitrogen cycle. Earth-Science Reviews.
Ranjan, S., & Sasselov, D. D. (2017). Constraints on the early terrestrial nitrogen cycle from photochemistry and atmospheric chemistry, Icarus.
Stüeken, E. E., Buick, R., Guy, B. M., & Koehler, M. C. (2015).
Isotopic evidence for biological nitrogen fixation by molybdenum-nitrogenase from 3.2 Ga,
Nature. ↩︎ - Bernard Marty (2012),The origins and concentrations of water, carbon, nitrogen and noble gases on Earth, Earth and Planetary Science Letters.
Vincent Busigny & Gray E. Bebout (2013).Nitrogen in the Earth: abundance and transport, Elements.
Halama, R., Bebout, G. E., et al. (2021). Nitrogen cycling in the Earth’s interior, Space Science Reviews. ↩︎ - L’azote possède une grande diversité d’états d’oxydation (de –3 dans l’ammoniac à +5 dans les nitrates). Les micro-organismes utilisent ces transformations comme une “chaîne énergétique” : certains oxydent l’azote (= produisent de l’énergie) , d’autres le réduisent (= utilisent d’autres sources d’énergie) . C’est l’équivalent, pour l’azote, de ce que la respiration est pour l’oxygène. ↩︎
- Ward & Jensen (2014), The microbial nitrogen cycle, Frontiers in microbiology. ↩︎
- Zhang et al. (2020), Global Nitrogen Cycle : critical enzymes, organisms, and processes for nitrogen budgets and dynamics, ACS publications. ↩︎
- Un équilibre redox décrit la balance entre les réactions d’oxydation (perte d’électrons) et de réduction (gain d’électrons) dans un milieu donné. Par exemple, la nitrification nécessite un milieu oxydant pour transférer des électrons de NH₃ vers l’oxygène, tandis que la dénitrification se produit dans des milieux réducteurs ou anoxiques, où les bactéries utilisent les nitrates comme accepteurs d’électrons. Les conditions redox locales déterminent donc quelles transformations de l’azote sont possibles à un moment donné. ↩︎
- LisaY.Stein , Martin G.Klotz (2016), The nitrogen cycle, Current biology. ↩︎
- Ward & Jensen. (2014). Op.cité. ↩︎
- Fowler et al.(2013), The global nitrogen cycle in the 21st century, The royal society publishing. ↩︎
- Zhang et al. (2020), Op.cité. ↩︎
- Ward & Jensen (2014). Op . cité ↩︎
- Cf note précédente – 7 ↩︎
- Vaclav Smil. Enriching the Earth: Fritz Haber, Carl Bosch, and the Transformation of World Food Production, MIT Press, 2001 (réédition 2004). ↩︎
- Pendant des milliards d’années, les flux d’azote. réactifs annuels se mesuraient en fractions de gigatonne. Ils s’élèvent aujourd’hui à environ 0,4 Gt N/an. En un siècle, l’humanité a ajouté 0,2 Gt N/an supplémentaires. Le procédé Haber-Bosch représente à lui seul environ 0,12 Gt N/an. Voir Fowler et al.(2013), op. cité. ↩︎
- Richardson, K. et al. (2023), Earth beyond six of nine planetary boundaries, Science Advances. ↩︎
Images : Partie 3 : U.S. Environmental Protection Agency, Public domain, via Wikimedia Commons / traduction svg via wikimedia ; étiquette : création AuM tous droits Alain Grandjean



Laisser un commentaire